Orage rythmique
1. Définition et pronostic
Le terme « orage rythmique » est né dans les années 1990 pour désigner des arythmies ventriculaires récidivantes sur une courte période de temps. L’orage rythmique est communément défini par la survenue d’au moins 3 tachycardies ventriculaires soutenues ou fibrillations ventriculaires en moins de 24h, chez les patients porteurs de DAI les épisodes doivent être séparés d’un moins 5 minutes[1]. Cette définition regroupe des situations cliniques très diverses, avec des formes paucisymptomatiques (TV réduites par ATP chez un porteur de DAI), mais aussi des formes très sévères engageant rapidement le pronostic vital (patients intubés en choc cardiogénique sur des arythmies ventriculaires réfractaires).
Le risque d’orage rythmique chez les patients porteurs de DAI est estimé à 10%/an chez les patients implantés en prévention secondaire et 1-2%/an chez les patients implantés en prévention primaire.
Le pronostic de l’orage rythmique est sombre, avec une mortalité estimée à 10-20% à 48h, et un risque de récurrence de plus de 50% dans l’année en l’absence d’ablation[2]. On ignore si l’orage rythmique est la conséquence d’une cardiopathie structurelle avancée évoluant vers l’insuffisance cardiaque terminale, ou s’il s’agit de la cause de la dégradation de la fonction cardiaque.
2. Étiologies et facteurs déclenchants
La physiopathologie de l’orage rythmique implique les 3 composantes du triangle de Coumel :
- Substrat électrophysiologique: cardiopathie structurelle ou non
- Facteur déclenchant : ischémie myocardique aigue, décompensation cardiaque, hypokaliémie, hyperthyroïdie, inobservance thérapeutique, traitements arythmogènes
- Dysrégulation du système nerveux autonome : augmentation du tonus sympathique
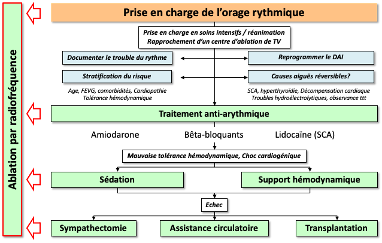
3. Prise en charge
A. Hospitalisation en unité de soins intensifs
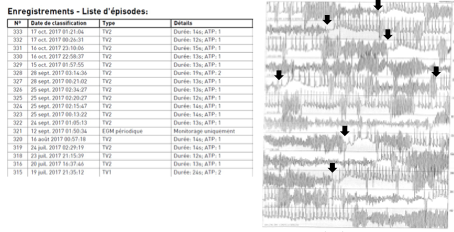
Le patient doit être pris en charge dans un service de soins intensifs cardiologiques ou de réanimation. La caractérisation des troubles du rythme est un enjeu majeur, notamment pour préparer une éventuelle procédure d’ablation. Il faut s’attacher à enregistrer des ECG 12 dérivations des épisodes de TV.
Les facteurs déclenchants doivent être recherchés et traités.
B. Reprogrammation du DAI
Le DAI doit être reprogrammé afin d’éviter les chocs électriques délivrés par l’appareil chez un patient encore vigile, source de stress majeure. Selon les situations, il faut envisager soit la désactivation complète des thérapies (par reprogrammation ou par l’application d’un aimant), soit la reprogrammation en allongeant les temps de détection et en augmentant les stimulations anti-tachycardiques afin d’éviter tout choc vigile. Il peut parfois être pertinent d’accélérer la fréquence de base afin d’éviter les alternances cycle long / cycle court.
C. Prise en charge psychologique
Les chocs itératifs et la situation d’urgence générée à chaque nouvelle arythmie vont avoir tendance à entretenir une hyperactivité sympathique chez le patient. Une anxiolyse per os ou IV est recommandée afin de contrer cette hypertonie sympathique pro-arythmique.
D. Traitement anti-arythmique
Différents médicaments anti-arythmiques sont essentiels dans la prise en charge de l’orage rythmique, attention néanmoins à l’administration concomitante de plusieurs anti-arythmiques ayant aussi un effet inotrope négatif, pouvant parfois précipiter le patient en choc cardiogénique[3].
a. Bêtabloquants
Les bêta-bloquants non cardiosélectifs (tels que le propranolol) semblent plus efficaces que les bêta-bloquants cardiosélectifs dans la prise en charge de l’orage rythmique. Il existe néanmoins toujours un risque de mauvaise tolérance hémodynamique, nous amenant souvent à privilégier des bêta-bloquants à courte demi-vie d’élimination, tels que l’esmolol (BREVIBLOCÒ).
b. Amiodarone
L’amiodarone est un anti-arythmique de classe III dans la classification de Vaughan-Williams, extrêmement efficace pour traiter les arythmies ventriculaires (40% d’efficacité sur les TV en monothérapie, plus de 50% en association à un bêta-bloquant, risque de récidive d’arythmie ventriculaire divisé par 4 si poursuite au-delà de la phase aiguë). L’amiodarone a un effet anti-arythmique par différentes voies : inhibition des canaux potassiques, mais aussi effet bêta-bloquant, inhibiteur des canaux sodiques et calciques. Il est recommandé de l’utiliser à forte dose dans la prise en charge de l’orage rythmique, et ce même chez des patients déjà sous amiodarone au long cours, elle est utilisable aussi ponctuellement même en cas d’antécédent d’hyperthyroïdie.
c. Lidocaïne
La lidocaïne est un anti-arythmique de classe Ib, surtout efficace en cas d’ischémie myocardique par une activité renforcée en situation de tachycardie, acidose, et réduction du potentiel transmembranaire. Hors contexte d’ischémie, son efficacité à réduire une TV monomorphe stable est estimée à 10 à 30%.
d. Sulfate de magnésium
Le sulfate de magnésium est indiqué uniquement en cas de torsade de pointes ou d’hypomagnésémie avérée.
E. Sédation
La sédation profonde est efficace via la diminution de l’activité nerveuse sympathique. Dans le cas d’un orage rythmique réfractaire aux médicaments anti-arythmiques, la moitié des patients sont contrôlés sur le plan rythmique dans les 15 minutes suivant la sédation. C’est un facteur pronostique majeur de mortalité hospitalière[4]. Il ne faut cependant pas oublier les complications inhérentes à la sédation et l’intubation, devant faire réserver cette prise en charge à des patients présentant de véritables arythmies ventriculaires récidivantes et réfractaires aux médicaments anti-arythmiques.
F. Neuromodulation
Le système nerveux autonome joue un rôle majeur dans la genèse et la récidive des arythmies ventriculaires, par l’hyperactivité sympathique générée par les chocs électriques répétés notamment. L’innervation sympathique du cœur provient de la partie inférieure du ganglion stellaire, et des ganglions T2, T3 et T4. Différentes approches sont décrites pour moduler cette innervation[5] :
- Sympathectomie chirurgicale : résection de la moitié inférieure du ganglion stellaire et des chaines ganglionnaires thoraciques T2 à T4 par voie endoscopique
- Sympathectomie percutanée : bloc du ganglion stellaire par injection d’un anesthésique local sous guidage échographique
- Anesthésie épidurale thoracique
- Dénervation rénale
G. Sonde d’entrainement
Lorsque la fréquence cardiaque de base est lente, avec de nombreuses ESV entrainant des alternances de cycles longs / cycles courts déclenchant des TV ou FV (souvent torsades de pointes sur QT long), il peut être utile de monter une sonde d’entrainement afin d’accélérer la fréquence de base.
H. Ablation par radiofréquence
L’ablation par radiofréquence est devenue, en association avec les médicaments anti-arythmiques, une pierre angulaire de la prise en charge de l’orage rythmique, il faut savoir l’évoquer suffisamment tôt dans la prise en charge. La procédure consiste en l’ablation de l’ensemble du substrat, potentiels tardifs et électrogrammes anormaux. Lorsque la procédure est efficace, la morbidité et la mortalité sont drastiquement réduites[6]. Le taux de succès de l’ablation en contexte d’orage rythmique reste néanmoins inférieur au taux de succès hors contexte d’orage rythmique (procédures plus complexes et plus longues, instabilité hémodynamique…).
I. Assistance circulatoire temporaire
La mise en place d’une ECMO (Extracorporeal Membrane Oxygenation) peut s’avérer nécessaire lorsque les troubles du rythme restent réfractaires aux anti-arythmiques et à la sédation profonde. L’ECMO est efficace dans 2/3 des cas environ dans ces situations, grâce à la décharge ventriculaire gauche[7]. Elle peut permettre aussi de stabiliser l’hémodynamique et permettre une procédure d’ablation. Il s’agit néanmoins d’une solution de dernier recours, avec des complications fréquentes et graves.
J. Assistance ventriculaire gauche et transplantation
Chez des patients jeunes présentant des arythmies ventriculaires récidivantes et réfractaires aux différentes thérapeutiques sus-citées, la mise en place d’une assistance ventriculaire gauche ou la transplantation cardiaque peuvent être envisagées, il s’agit souvent de patients à l’hémodynamique instable, avec d’autres défaillances d’organes, et la morbimortalité reste très élevée dans cette population[8].
K. Cas particuliers
a. Syndrome de Brugada
L’isoprénaline IVSE est efficace dans les orages rythmiques du syndrome de Brugada, elle peut être relayée par de la quinidine per os. L’ablation radiofréquence de l’infundibulum pulmonaire par voie épicardique a également démontré son efficacité.
b. Syndrome du QT long
Les bêta-bloquants et la flécaïne sont efficaces, de même que la supplémentation en Mg et potassium. On peut être amené à monter une sonde d’entrainement pour accélérer la fréquence cardiaque de base, on peut proposer également en 2nde intention une sympathectomie.
c. Syndrome du QT court
La quinidine est le seul anti-arythmique ayant démontré son efficacité.
d. Syndrome de repolarisation précoce
Comme pour le syndrome de Brugada, l’isoprénaline et la quinidine sont efficaces.
e. TV polymorphes catécholergiques
Comme pour le syndrome du QT long, les bêta-bloquants et la flécaïne sont efficaces.
Références
- ↑ Al-Khatib SM, Stevenson WG, Ackerman MJ, Bryant WJ, Callans DJ, Curtis AB, et al. 2017 AHA/ACC/HRS Guideline for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death. Circulation. 2018 Sep 25;138(13):e272–391
- ↑ Guerra F, Shkoza M, Scappini L, Flori M, Capucci A. Role of electrical storm as a mortality and morbidity risk factor and its clinical predictors: a meta-analysis. EP Eur. 2014 Mar 1;16(3):347–53
- ↑ Geraghty L, Santangeli P, Tedrow UB, Shivkumar K, Kumar S. Contemporary Management of Electrical Storm. Heart Lung Circ. 2019 Jan 1;28(1):123–33.
- ↑ Martins RP, Urien JM, Barbarot N, Rieul G, Sellal JM, Borella L, Clementy N, Bisson A, Guenancia C, Sagnard A, Schumacher S, Gandjbakhch E, Duchateau J, Tixier R, Goepp A, Hamon D, Lellouche N, Champ-Rigot L, Milliez P, Marijon E, Varlet E, Garcia R, Degand B, Bouju P, Mabo P, Leclercq C, Behar N, Pavin D, de Chillou C, Sacher F, Galand V. Effectiveness of Deep Sedation for Patients With Intractable Electrical Storm Refractory to Antiarrhythmic Drugs. Circulation. 2020 Oct 20;142(16):1599-1601. doi: 10.1161/CIRCULATIONAHA.120.047468. Epub 2020 Oct 19. PMID: 33074763.
- ↑ Zhu C, Hanna P, Rajendran PS, Shivkumar K. Neuromodulation for Ventricular Tachycardia and Atrial Fibrillation: A Clinical Scenario-Based Review. JACC Clin Electrophysiol. 2019 Aug;5(8):881-896. doi: 10.1016/j.jacep.2019.06.009. Epub 2019 Aug 19. PMID: 31439288; PMCID: PMC6773263.
- ↑ Vergara P, Tung R, Vaseghi M, Brombin C, Frankel DS, Di Biase L, Nagashima K, Tedrow U, Tzou WS, Sauer WH, Mathuria N, Nakahara S, Vakil K, Tholakanahalli V, Bunch TJ, Weiss JP, Dickfeld T, Vunnam R, Lakireddy D, Burkhardt JD, Correra A, Santangeli P, Callans D, Natale A, Marchlinski F, Stevenson WG, Shivkumar K, Della Bella P. Successful ventricular tachycardia ablation in patients with electrical storm reduces recurrences and improves survival. Heart Rhythm. 2018 Jan;15(1):48-55. doi: 10.1016/j.hrthm.2017.08.022. Epub 2017 Aug 24. Erratum in: Heart Rhythm. 2018 Feb 5;: PMID: 28843418.
- ↑ Le Pennec-Prigent S, Flecher E, Auffret V, Leurent G, Daubert JC, Leclercq C, Mabo P, Verhoye JP, Martins RP. Effectiveness of Extracorporeal Life Support for Patients With Cardiogenic Shock Due To Intractable Arrhythmic Storm. Crit Care Med. 2017 Mar;45(3):e281-e289. doi: 10.1097/CCM.0000000000002089. PMID: 27755013.
- ↑ Martins RP, Hamel-Bougault M, Bessière F, Pozzi M, Extramiana F, Brouk Z, Guenancia C, Sagnard A, Ninni S, Goemine C, Defaye P, Boignard A, Maille B, Gariboldi V, Baudinaud P, Martin AC, Champ-Rigot L, Blanchart K, Sellal JM, De Chillou C, Dyrda K, Jesel-Morel L, Kindo M, Chaumont C, Anselme F, Delmas C, Maury P, Arnaud M, Flecher E, Benali K. Heart transplantation as a rescue strategy for patients with refractory electrical storm. Eur Heart J Acute Cardiovasc Care. 2023 Jun 15:zuad063. doi: 10.1093/ehjacc/zuad063. Epub ahead of print. PMID: 37319361.